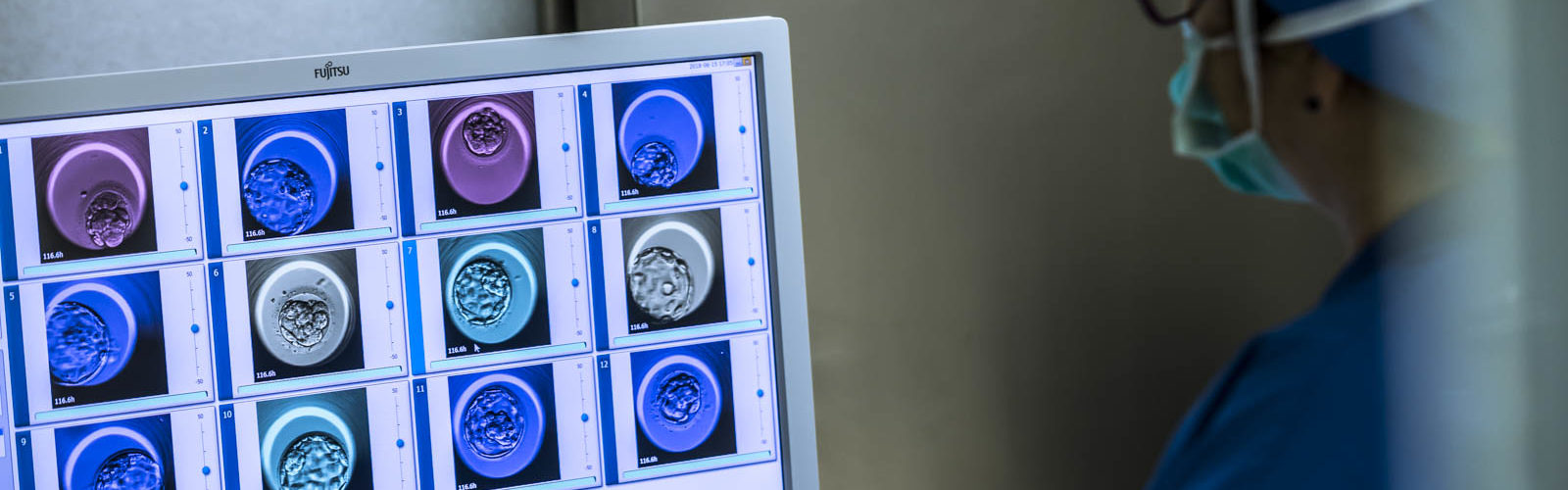
- La aneuploidía representa aproximadamente el 50% de las pérdidas precoces de embarazo
- El método IVC de cultivo de embriones humanos es una plataforma fiable para estudiar la capacidad de desarrollo temprano después de la implantación
El ser humano es el ser menos fértil que existe. A día de hoy, se cree que la aneuploidía, es decir, la presencia de un número anormal de cromosomas, es una de las principales limitaciones de la reproducción humana, pues representa aproximadamente el 50% de las pérdidas precoces de embarazo. Además, las tasas de aneuploidía son notablemente altas en embriones humanos fecundados in vitro, de los que hasta un 50% son diagnosticados como embriones aneuploides, según muestran las pruebas genéticas de preimplantación para detectar aneuploidías (PGT-A). Sin embargo, aún no hay información científica suficiente acerca del efecto que tiene cada aneuploidía específica sobre el desarrollo del embrión.
“Aquí nace nuestro estudio, elaborado junto a la doctora Magdalena Zernicka-Goetz, de la Universidad de Cambridge, cuyos resultados nos permiten presentar el primer análisis detallado del desarrollo posterior a la implantación de embriones humanos aneuploides. Consideramos prioritario estudiar para optimizar la práctica clínica en todos nuestros centros, ofreciendo así los mejores resultados a nuestros pacientes, una máxima para IVI. En esta línea, hallamos que la plataforma de cultivo de la Universidad de Cambridge es un excelente sistema donde estudiar el desarrollo embrionario y validar las pruebas genéticas de preimplantación”, comenta el doctor Antonio Pellicer, Presidente de IVIRMA Global, respaldado también por los doctores Emre Seli y Richard T. Scott Jr.
Las aneuploidías pueden provocar fallos en la implantación, abortos espontáneos y defectos congénitos. Dado que se sabe muy poco sobre el impacto de aneuploidías específicas durante las primeras etapas del desarrollo del embrión humano, el punto exacto en el que los embriones con células aneuploides cesan su desarrollo sigue sin estar claro. Esta falta de conocimiento se debe en gran parte a los desafíos técnicos en el estudio del desarrollo del embrión humano más allá de la implantación (día 7 desde la fecundación), un período que implica un crecimiento intensivo, remodelación celular y cambios en la identidad y el destino de las células madre. Los avances técnicos recientes han permitido que los embriones humanos se desarrollen más allá del día 7 y hasta el día 12 o 13 en el laboratorio, en ausencia de tejidos maternos. Los embriones cultivados en este sistema recapitulan las principales transformaciones morfológicas que los embriones desarrollan in vivo, por lo que este método de cultivo ofrece una oportunidad sin precedentes para caracterizar el desarrollo temprano posterior a la implantación de embriones humanos aneuploides en el laboratorio.
“Estos hallazgos evidencian, por ejemplo, cómo los embriones con trisomías 15 y 21 – es decir, que tienen tres copias de cada uno de estos cromosomas –, se desarrollan de manera similar a los embriones euploides – embriones normales que contienen dos copias de cada uno de los 23 cromosomas –, contrariamente a los embriones con monosomía 21 – una sola copia de este cromosoma –, los cuales muestran altas tasas de detención del desarrollo. Además, descubrimos tres casos de mosaicismo – una alteración en el número de cromosomas tan solo en algunas células del embrión – en embriones que inicialmente habían sido identificados como completamente aneuploides mediante PGT-A, destacando el potencial de nuestra plataforma de embriones humanos para determinar el alcance del mosaicismo genético y su influencia en el desarrollo humano posterior a la implantación”, explica el Dr. Pellicer.
El estudio, publicado recientemente en la prestigiosa revista científica Nature Communications, analiza los primeros 5 o 6 días del desarrollo de 9.803 embriones que mostraron una aneuploidía cromosómica, y los compara con 25.368 embriones euploides. El objetivo de esto es caracterizar el desarrollo de embriones humanos aneuploides en el laboratorio para descubrir los defectos celulares y de desarrollo de aneuploidías específicas y los mecanismos moleculares responsables.
“En resumen, el método IVC de cultivo de embriones humanos es una plataforma útil para estudiar la competencia del desarrollo temprano después de la implantación, un período del desarrollo embrionario que no se puede estudiar en embriones que se desarrollan in vivo. Utilizando este sistema, hemos detallado el desarrollo de embriones con aneuploidías específicas hasta el día 9 y las alteraciones específicas de los tejidos resultantes. Además, nuestros resultados demuestran que la plataforma de cultivo se puede utilizar para identificar casos de mosaicismo y embriones mal diagnosticados por PGT-A, lo cual abre la puerta a estudios futuros enfocados a determinar el destino de las células aneuploides durante el desarrollo temprano posterior a la implantación y la capacidad de desarrollo de los embriones mosaico, una necesidad clínica actualmente insatisfecha en la reproducción humana”, concluye el Dr. Pellicer.
