El Test Genético Preimplantacional (PGT) detecta y previene la transmisión a la descendencia de enfermedades graves causadas por alteraciones genéticas y cromosómicas en los embriones, antes de su implantación, para lograr que los hijos nazcan libres de enfermedades hereditarias.
El Test Genético Preimplantacional (PGT, por sus siglas en inglés) es el estudio genético que permite detectar alteraciones genéticas y cromosómicas en los embriones antes de su transferencia al útero minimizando el riesgo genético en la descendencia.
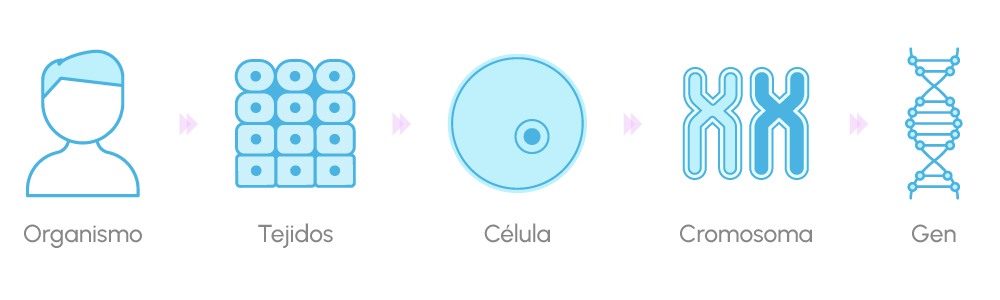
Los cromosomas son estructuras que se encuentran en el interior de cada célula y contienen la información genética, nuestro ADN. Los genes a su vez son segmentos de ADN que contienen la información sobre cómo deben funcionar las células del organismo.
El ser humano tiene 23 pares de cromosomas: 22 autosomas y un par de cromosomas sexuales (XX en el caso de las mujeres y XY en el caso de los hombres).
Con la fecundación del óvulo por el espermatozoide, cada uno de los progenitores aporta un cromosoma de cada par, y, así, se transmite nuestra herencia.

Sin embargo, en ocasiones se producen cambios que pueden dar lugar a una alteración cromosómica.
Las alteraciones pueden ser de dos tipos: numéricas (cuando hay cromosomas de más o de menos) y estructurales (cuando falta o sobra una parte de un cromosoma en particular, se ha pasado a otro o está invertida).
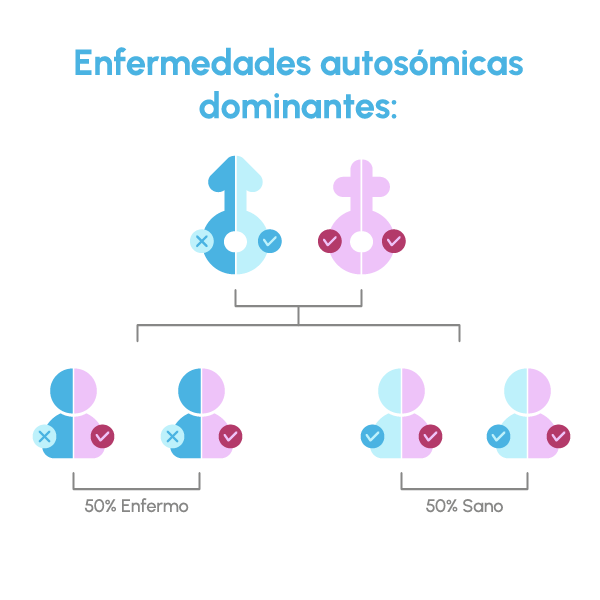
Otras veces, la alteración ocurre en un gen específico, lo que se conoce como alteración monogénica, y eso afecta al funcionamiento del organismo, dando lugar a una enfermedad. Estas enfermedades se pueden transmitir a la descendencia de diferentes maneras.
Cada tipo de PGT tiene sus peculiaridades, pero en todos ellos es necesario realizar un ciclo de fecundación in vitro para poder analizar genéticamente los embriones resultantes.


Después de la primera visita y tras 15-25 días de estimulación ovárica controlada, se procede a la obtención de los óvulos. Una vez fecundados con el semen del donante o de la pareja, se cultivan los embriones hasta blastocisto, para extraer un pequeño número de células de cada uno de los embriones y se procesan para su análisis genético. Ese mismo día se congelan los embriones biopsiados a la espera de resultados.
Una vez obtenido el informe de resultados y cuando ya sabemos cuáles de los embriones son aptos para ser transferidos se procede a la desvitrificación de uno de ellos y su transferencia al útero. El resto de los embriones normales quedarían congelados para un posible uso futuro.
Permite detectar si hay cromosomas de más o de menos en los embriones, lo que se conoce como alteración numérica.
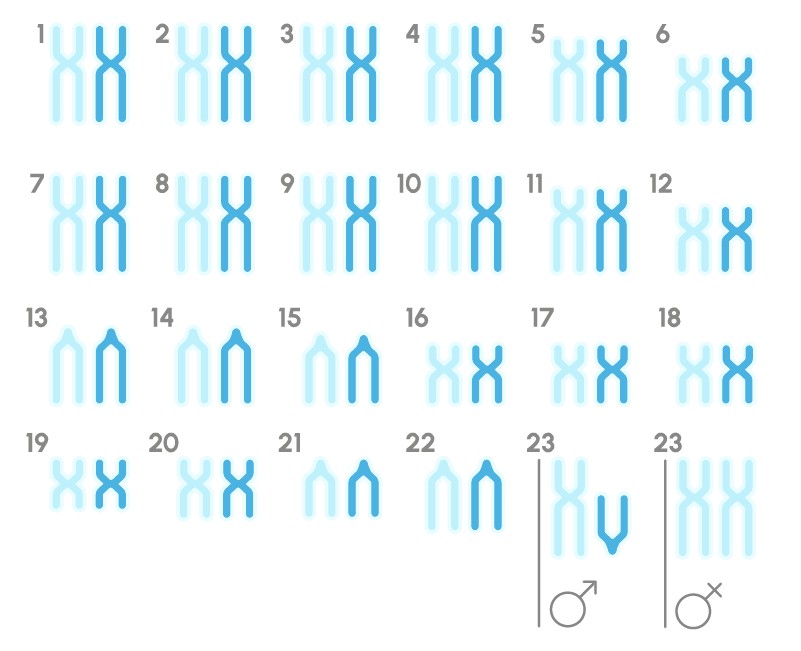
Permite detectar la alteración o mutación de un gen en concreto en los embriones que causaría una enfermedad monogénica o mendeliana. Este test analiza diferentes tipos de enfermedades hereditarias (autosómicas recesivas, autosómicas dominantes y enfermedades ligadas al cromosoma X).
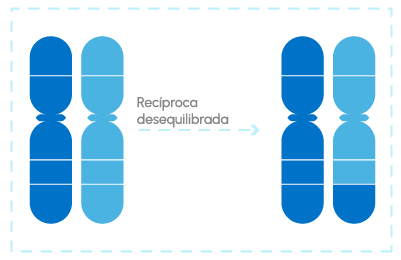
Permite detectar en los embriones la presencia de cromosomas anómalos por la ruptura o unión incorrecta de varios segmentos. Existen muchos tipos de anomalías cromosómicas estructurales; translocaciones, deleciones, duplicaciones, inserciones, anillaciones e inversiones, que en ocasiones pueden quedar equilibradas o no, algo que se conoce como alteraciones en desequilibrio.
Aquellos casos en los que debido a la alteración en la estructura de cromosoma el gen no se expresa correctamente tienen como resultado una enfermedad.
Delecciones: Una porción de uno de los cromosomas, al romperse y tratar de reconstruirse, se pierde, de manera que los genes que estuviesen en esa zona se ven afectados.
Duplicaciones: Un segmento de un cromosoma se duplica, de modo que hay una ganancia de los genes de esa región.
Inserciones: Un fragmento de un cromosoma se desprende de su lugar original y se inserta dentro de otro cromosoma.
Anillaciones: Un fragmento de uno de los cromosomas de la pareja se rompe en sus extremos y trata de repararse uniéndolos entre sí, formando un anillo; en esa reparación se dejan fuera dos porciones, que se pierden. Los genes que se encontraban en ese cromosoma no pueden seguir funcionando con normalidad, por lo que da lugar a una enfermedad.
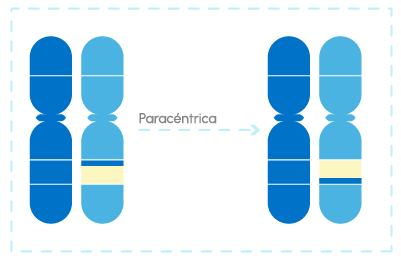
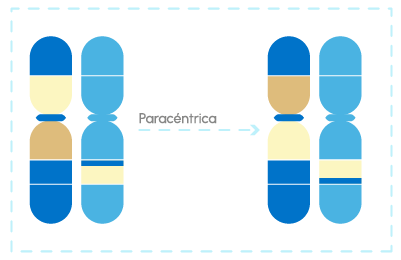
Inversiones: en una porción de uno de los cromosomas, se producen dos roturas, una porción gira y se vuelven a unir. Según el tipo de unión, esa rotura puede quedar reparada (equilibrada) o no.